Klant login
Log in
Registreer
Het aanmaken van een account heeft vele voordelen:
- Bekijk bestelling en verzendstatus
- Bekijk bestelgeschiedenis
- Reken sneller af
Winkelwagen
Subtotaal winkelwagen
U heeft geen product(en) in uw winkelwagen.
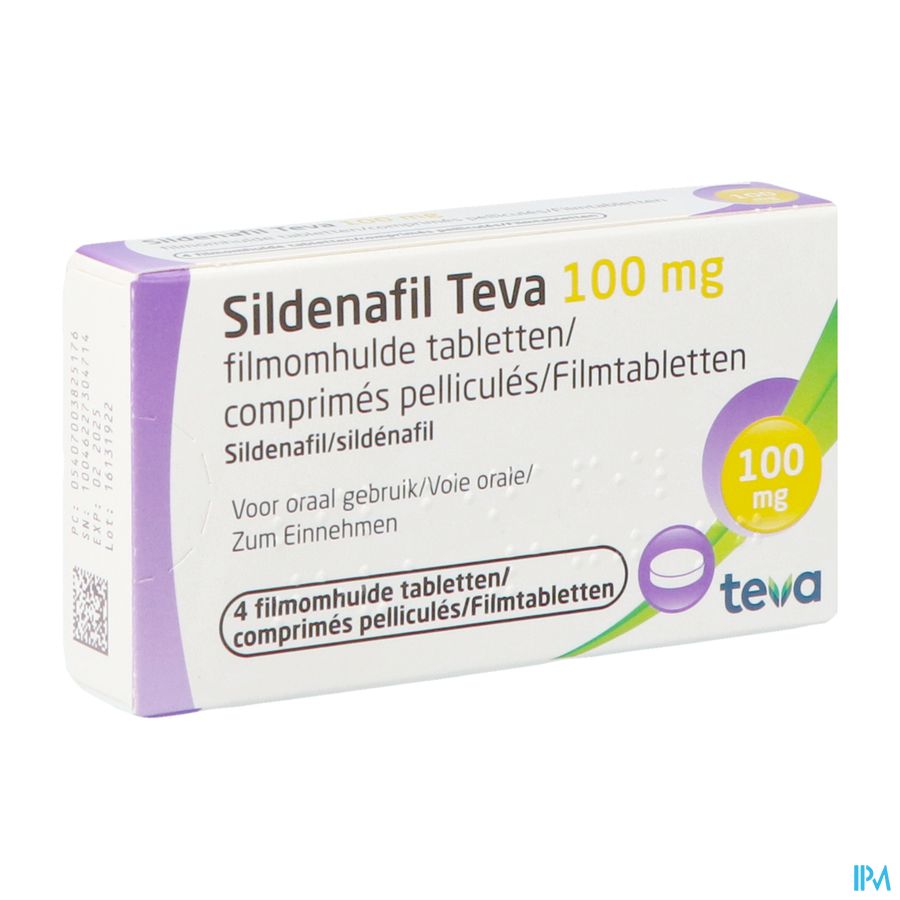
Sildenafil Teva 100mg Filmomh Tabl 4x 100mg
Terugbetaalbaar
Als je recht hebt op een terugbetaling voor dit geneesmiddel, betaal je in de apotheek een verlaagde prijs en niet de prijs die op onze webshop vermeld staat.
Terugbetalingstarief
€ 15,37 (6% inclusief btw)
Verhoogde tegemoetkoming
€ 15,37 (6% inclusief btw)
Dit product moet worden goedgekeurd door de apotheker.
Belangrijke informatie
Voor dit geneesmiddel is een voorschrift nodig. Na beoordeling door de apotheker kan je het komen afhalen en betalen in de apotheek.
Maximum toegelaten hoeveelheid in winkelwagen bereikt
Op bestelling
4.4 Bijzondere waarschuwingen en voorzorgen bij gebruik Er dient een anamnese te worden afgenomen en lichamelijk onderzoek te worden uitgevoerd om de diagnose erectiestoornis te bevestigen en om eventuele onderliggende oorzaken vast te stellen, voordat farmacologische behandeling wordt overwogen. Cardiovasculaire risicofactoren Er is een gering cardiaal risico verbonden aan seksuele activiteit. Daarom dienen artsen te overwegen de cardiovasculaire conditie van patiënten te onderzoeken vóór aanvang van de behandeling van erectiestoornissen. Sildenafil heeft vaatverwijdende eigenschappen, waardoor milde en voorbijgaande verlaging van de bloeddruk kan optreden (zie rubriek 5.1). Voordat sildenafil wordt voorgeschreven, dienen artsen zorgvuldig te overwegen of hun patiënten, met bepaalde onderliggende aandoeningen, ongewenste gevolgen kunnen ondervinden door dergelijke vaatverwijdende effecten; vooral in combinatie met seksuele activiteit. Patiënten die gevoeliger zijn voor vaatverwijders zijn onder andere patiënten met linker ventrikel outflow obstructie (zoals aortastenose, hypertrofische obstructieve cardiomyopathie) of met het zeldzame syndroom van multipel systeem atrofie wat zich uit als ernstig gestoorde autonome controle van de bloeddruk. Sildenafil Teva versterkt het hypotensieve effect van nitraten (zie rubriek 4.3). Ernstige cardiovasculaire voorvallen, waaronder myocardinfarct, instabiele angina, plotselinge hartdood, ventriculaire aritmie, cerebrovasculaire hemorrhagie, transiënte ischemische aanvallen, hypertensie en hypotensie zijn in post-marketing surveillance gemeld in de tijdsspanne waarin sildenafil gebruikt werd. De meeste maar niet al deze patiënten vertoonden preëxistente cardiovasculaire risicofactoren. Vele voorvallen traden op tijdens of kort na seksuele activiteit en sommige kort na gebruik van sildenafil zonder seksuele activiteit. Het is onmogelijk om na te gaan of deze voorvallen rechtstreeks verband houden met deze factoren of andere factoren. Priapisme Geneesmiddelen voor de behandeling van erectiestoornissen, waaronder sildenafil, moeten voorzichtig worden toegepast bij patiënten met anatomische deformatie van de penis (zoals angulatie, fibrose van de corpora cavernosa of de ziekte van Peyronie) of bij patiënten met aandoeningen die kunnen predisponeren tot het optreden van priapisme (zoals sikkelcelanemie, multipel myeloom of leukemie). Uit postmarketingervaring met sildenafil zijn lang aanhoudende erecties en priapisme gemeld. Wanneer een erectie langer dan 4 uur aanhoudt, dient de patiënt onmiddellijk medische hulp in te roepen. Als priapisme niet onmiddellijk wordt behandeld, kan dit leiden tot beschadiging van het penisweefsel en permanent verlies van de potentie. Gelijktijdig gebruik met andere PDE5-remmers of andere behandelingen voor erectiestoornissen De veiligheid en werkzaamheid van sildenafil in combinatie met andere PDE5-remmers, of andere geneesmiddelen ter behandeling van pulmonale arteriële hypertensie (PAH) die sildenafil bevatten, of andere behandelingswijzen van erectiestoornissen zijn niet onderzocht. Daarom wordt het gebruik van dergelijke combinaties afgeraden. Effecten op het gezichtsvermogen Voorvallen van visusstoornissen zijn spontaan gemeld in relatie met de inname van sildenafil en andere PDE5-remmers (zie rubriek 4.8). Voorvallen van non-arteritic anterior ischaemic optic neuropathy, een zeldzame aandoening, zijn spontaan en in een observationele studie gemeld in relatie met de inname van sildenafil en andere PDE5-remmers (zie rubriek 4.8). Patiënten dient te worden geadviseerd, om in geval van een plotselinge visusstoornis het gebruik van Sildenafil Teva stop te zetten en onmiddellijk een arts te raadplegen (zie rubriek 4.3). Gelijktijdig gebruik met ritonavir Gelijktijdige toediening van sildenafil met ritonavir wordt niet aangeraden (zie rubriek 4.5). Gelijktijdig gebruik met alfablokkers Voorzichtigheid is geboden wanneer sildenafil wordt toegediend aan patiënten die een alfablokker gebruiken, aangezien de gelijktijdige toediening tot symptomatische hypotensie kan leiden bij enkele individuen die hier gevoelig voor zijn (zie rubriek 4.5). De kans hierop is het grootst binnen 4 uur na toediening van sildenafil. Om de kans op het ontwikkelen van orthostatische hypotensie te minimaliseren dienen patiënten hemodynamisch stabiel op alfablokkertherapie te zijn ingesteld voordat wordt begonnen met de sildenafilbehandeling. Starten van de sildenafilbehandeling met een dosering van 25 mg dient te worden overwogen (zie rubriek 4.2). Bovendien dienen artsen hun patiënten te adviseren wat ze moeten doen wanneer er symptomen van orthostatische hypotensie ontstaan. Effect op bloeding Onderzoek met menselijke bloedplaatjes toont aan dat sildenafil de anticoagulerende werking van natriumnitroprusside in vitro versterkt. Er is geen informatie beschikbaar omtrent de veiligheid van sildenafil voor patiënten met stollingsstoornissen of een actief peptisch ulcus. Daarom dient sildenafil alleen te worden toegediend aan deze patiënten na zorgvuldige afweging van de voordelen en de risico's. Vrouwen Sildenafil Teva is niet geïndiceerd voor gebruik door vrouwen. Hulpstof Natrium Dit middel bevat minder dan 1 mmol natrium (23 mg) per filmomhulde tablet, dat wil zeggen dat het in wezen 'natriumvrij' is.
Sildenafil Teva is geïndiceerd voor gebruik bij volwassen mannen met erectiestoornissen, dit is hetonvermogen een erectie te krijgen en te behouden, voldoende voor bevredigende seksuele activiteit.
Voor de werkzaamheid van Sildenafil Teva is seksuele prikkeling noodzakelijk
Elke tablet bevat sildenafilcitraat overeenkomend met 100 mg sildenafil.
- Tabletkern:
Microkristallijne cellulose
Calciumwaterstoffosfaat watervrij
Croscarmellose natrium
Magnesiumstearaat
- Filmomhulling:
Polyvinylalcohol
Titaandioxide (E171)
Macrogol 3350
Talk
4.5 Interacties met andere geneesmiddelen en andere vormen van interactie Invloeden van andere geneesmiddelen op sildenafil In vitro onderzoek Sildenafil wordt hoofdzakelijk gemetaboliseerd via het cytochroom P450 (CYP) iso-enzym 3A4 (hoofdroute) en 2C9 (nevenroute). Om die reden kunnen remmers van deze iso-enzymen de klaring van sildenafil verminderen en kunnen inductoren van deze iso-enzymen de klaring van sildenafil vermeerderen. In vivo onderzoek Populatiefarmacokinetische analyse van de gegevens uit klinische studies gaf aan dat de sildenafilklaring werd verminderd bij een gelijktijdige toediening van CYP3A4-remmers (zoals ketoconazol, erytromycine en cimetidine). Alhoewel er geen toename van ongewenste voorvallen in deze patiënten werd gezien wanneer sildenafil tegelijkertijd met een CYP3A4-remmer werd toegediend, dient een startdosis van 25 mg te worden overwogen. Gelijktijdige toediening van de HIV-proteaseremmer ritonavir, die een zeer sterke remmer is van P450, bij een steady state (500 mg tweemaal daags) met sildenafil (100 mg, enkele dosis) resulteerde in een 300 % (4-voudige) verhoging van de Cmax van sildenafil en een 1.000 % (11-voudige) verhoging van de AUC van de sildenafil-plasmaspiegels. Na 24 uur waren de plasmaspiegels van sildenafil nog steeds ongeveer 200 ng/ml, vergeleken met ongeveer 5 ng/ml wanneer sildenafil alleen werd toegediend. Dit is in overeenstemming met de uitgesproken effecten van ritonavir op een groot aantal substraten van het cytochroom P450. Sildenafil had geen effect op de farmacokinetiek van ritonavir. Gebaseerd op deze farmacokinetische resultaten wordt gelijktijdige toediening van sildenafil met ritonavir niet aanbevolen (zie rubriek 4.4) en in geen geval mag de maximale dosis van sildenafil 25 mg per 48 uur overschrijden. Gelijktijdige toediening van de HIV-proteaseremmer saquinavir, een CYP3A4-remmer, bij steady state (1200 mg driemaal daags) met sildenafil (100 mg, enkele dosis) resulteerde in een 140 % stijging van de Cmax van sildenafil en een 210 % stijging van de AUC van sildenafil. Sildenafil had geen effect op de farmacokinetiek van saquinavir (zie rubriek 4.2). Van sterkere CYP3A4-remmers, zoals ketoconazol en itraconazol zou een groter effect verwacht kunnen worden. Wanneer een enkele 100 mg dosis sildenafil wordt toegediend met erytromycine, een matige CYP3A4-remmer, bij steady state (500 mg tweemaal daags gedurende 5 dagen), werd een stijging van 182 % gezien van de systemische sildenafil-blootstelling (AUC). In normale gezonde mannelijke vrijwilligers was er geen bewijs voor een effect van azitromycine (500 mg per dag, gedurende 3 dagen) op de AUC, Cmax, tmax, eliminatiesnelheidsconstante of de afgeleide halfwaardetijd van sildenafil of zijn belangrijkste circulerende metaboliet. Cimetidine (800 mg), een cytochroom P450- remmer en een niet-specifieke CYP3A4-remmer, veroorzaakte een stijging van de sildenafilplasmaconcentraties met 56 %, wanneer het gelijktijdig met sildenafil (50 mg) werd toegediend aan gezonde vrijwilligers. Grapefruitsap is een zwakke remmer van het CYP3A4-metabolisme in de darmwand en kan een lichte stijging van de sildenafil-plasmaspiegels veroorzaken. Een enkelvoudige dosis antacidum (magnesiumhydroxide/aluminiumhydroxide) had geen invloed op de biologische beschikbaarheid van sildenafil. Alhoewel er niet voor alle geneesmiddelen specifieke interactiestudies zijn uitgevoerd, bleek uit populatiefarmacokinetische analyses geen effect op de farmacokinetiek van sildenafil wanneer gelijktijdige behandeling werd toegepast met middelen uit de groep van CYP2C9-remmers (zoals tolbutamide, warfarine en fenytoïne), van CYP2D6-remmers (zoals selectieve serotonine�heropnameremmers, tricyclische antidepressiva), thiazide- en verwante diuretica, lis- en kaliumsparende diuretica, angiotensine converterend enzymremmers, calciumblokkers, bèta�adrenoreceptorantagonisten of middelen die het CYP450-metabolisme induceren (zoals rifampicine, barbituraten). In een studie bij gezonde mannelijke vrijwilligers resulteerde gelijktijdige toediening van de endotheline antagonist bosentan (een inductor van CYP3A4 (matig), CYP2C9 en mogelijk CYP2C19) bij steady state (125 mg tweemaal daags) met sildenafil bij steady state (80 mg driemaal daags) in een daling van 62,6% en 55,4% van respectievelijk sildenafil AUC en Cmax. Om die reden wordt verwacht dat gelijktijdige toediening van sterke CYP3A4-inductoren, zoals rifampine, zal leiden tot grotere dalingen in de plasmaconcentraties van sildenafil. Nicorandil is een hybride van een kaliumkanaalactivator en nitraat. Door de nitraatcomponent kan de stof leiden tot een ernstige interactie met sildenafil. Invloeden van sildenafil op andere geneesmiddelen In vitro onderzoek: Sildenafil is een zwakke remmer van cytochroom P450 in de isovormen 1A2, 2C9, 2C19, 2D6, 2E1 en 3A4 (IC50 > 150 μM). Gezien de maximale plasmaconcentraties van sildenafil van ongeveer 1 μM na inname van de aanbevolen dosis, is het onwaarschijnlijk dat Sildenafil Teva de klaring zal veranderen van substraten voor deze iso-enzymen. Er zijn geen gegevens over de interactie van sildenafil met niet-specifieke fosfodiësteraseremmers, zoals theofylline of dipyridamol. In vivo onderzoek: In overeenstemming met het effect op het stikstofoxide/cGMP mechanisme (zie rubriek 5.1), gaf sildenafil een potentiëring van de hypotensieve effecten van nitraten. Gelijktijdige toediening van middelen die stikstofoxide afgeven of nitraten, in welke vorm dan ook, is daarom gecontra-indiceerd (zie rubriek 4.3). Riociguat: Preklinische studies toonden een additief systemisch bloeddrukverlagend effect aan als PDE5-remmers werden gecombineerd met riociguat. In klinische studies bleek riociguat het bloeddrukverlagend effect van PDE5-remmers te vergroten. Bij de bestudeerde populatie was er geen bewijs van een gunstig klinisch effect van de combinatie. Gelijktijdig gebruik van riociguat met PDE5-remmers, waaronder sildenafil, is gecontra-indiceerd (zie rubriek 4.3). Gelijktijdige toediening van sildenafil aan patiënten die alfablokkertherapie krijgen kan mogelijk leiden tot symptomatische hypotensie bij enkele individuen die hier gevoelig voor zijn. De kans hierop is het grootst binnen 4 uur na toediening van sildenafil (zie rubrieken 4.2 en 4.4). In drie specifieke geneesmiddelinteractiestudies werden de alfablokker doxazosine (4 mg en 8 mg) en sildenafil (25 mg, 50 mg of 100 mg) gelijktijdig toegediend aan patiënten met benigne prostaathyperplasie (BPH) die stabiel waren ingesteld op doxazosinetherapie. In deze studiepopulaties werden gemiddelde additionele bloeddrukdalingen in liggende positie waargenomen van respectievelijk 7/7 mmHg, 9/5 mmHg and 8/4 mmHg en gemiddelde additionele bloeddrukdalingen in stand van respectievelijk 6/6 mmHg, 11/4 mmHg en 4/5 mmHg. Wanneer sildenafil en doxazosine gelijktijdig werden toegediend aan patiënten die stabiel waren ingesteld op doxazosinetherapie, waren er zelden meldingen van patiënten die symptomatische orthostatische hypotensie hadden ondervonden. Deze meldingen omvatten duizeligheid en een licht gevoel in het hoofd, maar geen syncope. Er werden geen significante interacties aangetoond wanneer sildenafil (50 mg) gelijktijdig werd toegediend met tolbutamide (250 mg) of warfarine (40 mg), die beide worden gemetaboliseerd door CYP2C9. Sildenafil (50 mg) versterkte de toename van de stollingstijd veroorzaakt door acetylsalicylzuur (150 mg) niet. Sildenafil (50 mg) versterkte het hypotensieve effect van alcohol bij gezonde vrijwilligers met een gemiddelde maximum alcoholconcentratie in bloed van 80 mg/dl niet. Samenvoegen van de gegevens betreffende de volgende klassen antihypertensiva: diuretica, bètablokkers, ACE-remmers, angiotensine II antagonisten, (vasodilatoire en centraal werkende) antihypertensiva, adrenerge neuronblokkers, calciumantagonisten en alfa-adrenerge receptorblokkers gaf geen verschil in het bijwerkingenprofiel van patiënten die sildenafil toegediend kregen in vergelijking met patiënten behandeld met placebo. In een specifieke interactiestudie werd sildenafil (100 mg) gelijktijdig met amlodipine toegediend aan hypertensiepatiënten. Er werd een additionele systolische bloeddrukdaling waargenomen, in liggende positie, van 8 mmHg. De corresponderende additionele diastolische bloeddrukdaling, gemeten in liggende positie was 7 mmHg. Deze additionele bloeddrukdalingen waren in dezelfde orde van grootte als die gezien na toediening van alleen sildenafil aan gezonde vrijwilligers (zie rubriek 5.1). De toevoeging van een enkelvoudige dosis sildenafil aan sacubitril/valsartan in de 'steady state' bij patiënten met hypertensie werd geassocieerd met een significant grotere verlaging van de bloeddruk in vergelijking met de toediening van alleen sacubitril/valsartan. Daarom is voorzichtigheid geboden wanneer sildenafil wordt aangevangen bij patiënten die worden behandeld met sacubitril/valsartan. Sildenafil (100 mg) had geen effect op de steady state-farmacokinetiek van de HIV-proteaseremmers saquinavir en ritonavir, welke beide CYP3A4-substraten zijn. Bij gezonde mannelijke vrijwilligers resulteerde sildenafil bij steady state (80 mg driemaal daags) in een stijging van 49,8% van bosentan AUC en een stijging van 42% van bosentan Cmax (125 mg tweemaal daags).
4.8 Bijwerkingen Samenvatting van het veiligheidsprofiel Het veiligheidsprofiel van sildenafil is gebaseerd op 9.570 patiënten in 74 dubbelblinde placebo�gecontroleerde klinische studies. De vaakst gerapporteerde bijwerkingen in klinische studies bij patiënten die met sildenafil werden behandeld, waren hoofdpijn, blozen, dyspepsie, verstopte neus, duizeligheid, misselijkheid, opvliegers, visusverstoring, cyanopsie en onscherp zien. Bijwerkingen uit post-marketing surveillance zijn tijdens een geschatte periode >10 jaar bijeengebracht. Aangezien niet alle bijwerkingen aan de Houder van de vergunning voor het in de handel brengen worden gemeld en worden opgenomen in de veiligheidsdatabank, kunnen de frequenties van deze reacties niet betrouwbaar worden vastgesteld. Lijst van bijwerkingen in tabelvorm In onderstaande tabel zijn alle medisch belangrijke bijwerkingen, die optraden in klinische studies met een incidentie groter dan bij placebo, gerangschikt per systeem/orgaanklasse en frequentie (zeer vaak (≥1/10), vaak (≥1/100 tot <1/10), soms (≥1/1.000 tot <1/100), zelden (≥1/10.000 tot <1/1.000). Binnen elke frequentiegroep zijn de bijwerkingen gerangschikt naar afnemende ernst. Tabel 1: Medisch belangrijke bijwerkingen, gerapporteerd met een incidentie groter dan bij placebo in gecontroleerde klinische studies, alsmede medisch belangrijke bijwerkingen, gerapporteerd uit post-marketing surveillance. Systeem/Orgaanklasse Zeer vaak (≥1/10) Vaak (≥1/100, <1/10) Soms (≥1/1.000, <1/100) Zelden (≥1/10.000, <1/1.000) Infecties en parasitaire aandoeningen Rinitis Immuunsysteem�aandoeningen Overgevoeligheid Zenuwstelsel�aandoeningen Hoofdpijn Duizeligheid Slaperigheid, Hypo-esthesie Cerebrovasculair accident, Voorbijgaande ischemische aanval, Convulsie*, Herhaald optreden van convulsie*, Syncope Oogaandoeningen Afwijkingen in het kleuren�zien**, Visusver�storing, Onscherp zien Traanaandoe�ningen***, Oogpijn, Fotofobie, Fotopsie, Oculaire hyperemie, Visuele helderheid, Conjunctivitis Non-arteritic anterior ischaemic optic neuropathy (NAION)*, Retinale bloedvat�occlusie*, Retinale bloeding, Arteriosclerotisch e retinopathie, Retinale stoornis, Glaucoom, Gezichtsveld�defect, Diplopie, Verminderde gezichtsscherpte, Myopie, Asthenopie, Glasvochttroe�beling, Irisstoornis, Mydriasis, Halovisie, Oogoedeem, Oogzwelling, Oogaandoening, Conjunctivale hyperemie, Oogirritatie, Abnormaal gevoel in oog, Ooglidoedeem, Sclerale verkleuring Evenwichtsorgaan- en ooraandoeningen Vertigo, Tinnitus Doofheid Hartaandoeningen Tachycardie, Hartkloppingen Plotselinge hartdood*, Myocardinfarct, Ventriculaire aritmie*, Atriumfibrilleren, Instabiele angina Bloedvataandoeningen Blozen, Opvliegers Hypertensie, Hypotensie Ademhalingsstelsel-, borstkas- en mediastinumaandoening en Verstopte neus Epistaxis, Sinuscongestie Dichtgeknepen keel, Neusoedeem, Droge neus Maagdarmstelsel�aandoeningen Misselijk�heid, Dyspepsie Gastro�oesofageale refluxziekte, Braken, Pijn in de bovenbuik, Droge mond Orale hypo�esthesie Huid- en onderhuidaandoeningen Uitslag Stevens-Johnson syndroom (SJS)*, Toxische epidermale necrolyse (TEN)* Skeletspierstelsel- en bindweefsel�aandoeningen Myalgie, Pijn in de extremiteiten Nier- en urinewegaandoeningen Hematurie Voortplantingsstelsel�en borstaandoeningen Penisbloeding, Priapisme*, Hematospermie, Toegenomen erectie Algemene aandoeningen en toedieningsplaats�stoornissen Pijn op de borst, Vermoeidheid, Warm hebben Prikkelbaarheid Onderzoeken Verhoogde hartslag *Alleen melding tijdens postmarketingsurveillance ** Afwijkingen in het kleurenzien: Chloropsie, Chromatopsie, Cyanopsie, Erytropsie en Xanthopsie *** Traanaandoeningen: Droog oog, Lacrimale stoornis en Verhoogde tranenvloed Melding van vermoedelijke bijwerkingen Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico's van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het Nederlands Bijwerkingen Centrum Lareb, Website: www.lareb.nl.
4.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
In overeenstemming met zijn bekende effect op het stikstofmonoxide/cyclisch guanosinemonofosfaat (cGMP) mechanisme (zie rubriek 5.1), heeft sildenafil versterking van het hypotensieve effect van nitraten laten zien. Gelijktijdige toediening van stoffen die stikstofmonoxide afgeven (zoals amylnitriet) of nitraten, ongeacht welke vorm, is daarom gecontra-indiceerd.
Gelijktijdige toediening van PDE5-remmers, waaronder sildenafil, met guanylaatcyclasestimulatoren, zoals riociguat, is gecontra-indiceerd omdat het mogelijk kan leiden tot symptomatische hypotensie (zie rubriek 4.5).
Geneesmiddelen voor de behandeling van erectiestoornissen, waaronder sildenafil, dienen niet gebruikt te worden door mannen voor wie seksuele activiteit wordt afgeraden (bijvoorbeeld patiënten met ernstige cardiovasculaire stoornissen zoals instabiele angina of ernstig hartfalen).
Sildenafil Teva is gecontra-indiceerd bij patiënten met visusverlies in één oog als gevolg van een niet-arteriële anterieure ischemische opticoneuropathie (non-arteritic anterior ischaemic optic neuropathy, NAION), ongeacht of dit voorval gerelateerd was aan eerdere blootstelling aan een PDE5-remmer of niet (zie rubriek 4.4).
De veiligheid van sildenafil is niet onderzocht in de volgende patiëntengroepen en daarom is het gebruik gecontra-indiceerd bij: patiënten met ernstige leverfunctiestoornis, patiënten met hypotensie (bloeddruk < 90/50 mmHg), patiënten die recent een beroerte of een myocardinfarct hebben doorgemaakt en bij patiënten met erfelijke degeneratieve retinale stoornissen, zoals retinitis pigmentosa (een minderheid van deze patiënten heeft een genetische afwijking van retinale fosfodiësterases).
Sildenafil Teva is niet geïndiceerd voor gebruik door vrouwen. Er zijn geen adequate en goed gecontroleerde onderzoeken verricht bij zwangere vrouwen of vrouwen die borstvoeding geven. Er zijn geen relevante bijwerkingen met betrekking tot de voortplanting gevonden in studies met ratten en konijnen na orale toediening van sildenafil. Er was geen effect op de spermamotiliteit en -morfologie na enkelvoudige orale doses van 100 mg sildenafil bij gezonde vrijwilligers (zie rubriek 5.1).
Dosering
- Gebruik door volwassenen:
De aanbevolen dosis is 50 mg, in te nemen naar behoefte ongeveer één uur voorafgaand aan seksueleactiviteit. Op grond van de effectiviteit en de verdraagbaarheid kan de dosis worden verhoogd tot100 mg of worden verlaagd naar 25 mg. De maximaal aanbevolen dosis is 100 mg. De maximaalaanbevolen doseringsfrequentie is eenmaal per dag. Wanneer Sildenafil Teva tegelijk met voedselwordt ingenomen kan, ten opzichte van een nuchtere toestand, het intreden van de werking wordenvertraagd.
Speciale populaties
- Ouderen
Een aanpassing van de dosering is bij ouderen niet nodig (≥ 65 jaar).
- Verminderde nierfunctie
De aanbevolen doseringen beschreven bij 'Gebruik door volwassenen' zijn van toepassing oppatiënten met lichte tot matige nierfunctiestoornissen (creatinineklaring = 30-80 ml/min).
Daar de klaring van sildenafil verminderd is bij patiënten met ernstige nierfunctiestoornissen
(creatinineklaring < 30 ml/min) dient een dosering van 25 mg te worden overwogen. Gebaseerd op deeffectiviteit en de verdraagbaarheid, kan de dosis zo nodig stapsgewijs worden verhoogd tot 50 mg,maximaal 100 mg.
- Verminderde leverfunctie
Daar de klaring van sildenafil is verminderd bij patiënten met leverfunctiestoornissen (bijvoorbeeldcirrose), dient een dosis van 25 mg te worden overwogen. Gebaseerd op de effectiviteit en deverdraagbaarheid, kan de dosis worden verhoogd tot 50 mg, maximaal 100 mg.
- Gebruik bij patiënten die andere geneesmiddelen gebruiken
Met uitzondering van ritonavir, waarvoor gelijktijdige toediening met sildenafil niet wordt aanbevolen, dient een startdosis van 25 mg te worden overwogen bij patiënten die gelijktijdigworden behandeld met CYP3A4-remmers.
Om de kans op het ontwikkelen van orthostatische hypotensie bij patiënten die alfablokkerbehandelingkrijgen te minimaliseren, dienen patiënten op alfablokkertherapie te zijn gestabiliseerd voordat wordtbegonnen met de sildenafilbehandeling. Bovendien dient aanvang van de sildenafilbehandeling meteen dosering van 25 mg te worden overwogen.
Wijze van toediening
Voor oraal gebruik.
| CNK | 3008711 |
|---|---|
| Organisaties | Arega Pharma NV, Teva Belgium |
| Merken | Teva |
| Breedte | 55 mm |
| Lengte | 101 mm |
| Diepte | 20 mm |
| Hoeveelheid verpakking | 4 |
| Actieve ingrediënten | sildenafil citraat |
| Behoud | Kamertemperatuur (15°C - 25°C) |